FDA genehmigt Anti-sucht-Implantat um opioid Abhängigkeit zu verhindern
Das Implantat, Probuphine, verzichtet auf eine niedrige Dosis von Buprenorphin über einen Zeitraum von sechs Monaten und Befürworter hoffen, dass es die Chancen Missbrauch verringern würde
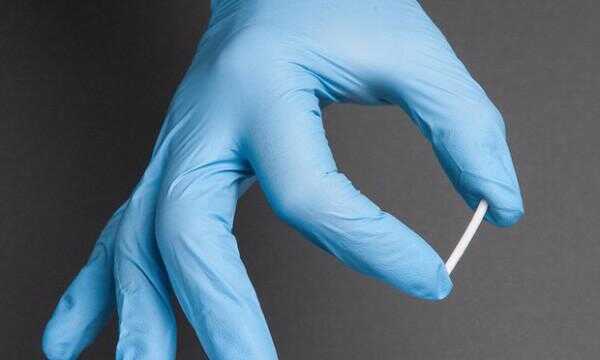
Die US Food and Drug Administration genehmigt die erste implantierbare Opioidabhängigkeit Behandlung am Donnerstag.
Diese Entscheidung wird wie die Obama-Administration Werke reagieren auf Amerikas Opioidabhängigkeit Epidemie – wo 80 Amerikaner sterben jeden Tag von Überdosierungen.
"Opioid Missbrauch und Abhängigkeit haben einen verheerenden auf amerikanische Familien Tribut gefordert. Müssen wir alles, was wir, um neue, innovative Behandlungsmöglichkeiten zur Verfügung zu stellen können, die Patienten wieder die Kontrolle über ihr Leben helfen können", sagte FDA Kommissar, Robert M Califf, in einer Erklärung.
Das Implantat, Probuphine, verzichtet eine niedrige Dosis des Anti-sucht Droge Buprenorphin kontinuierlich über einen Zeitraum von sechs Monaten. Es richtet sich an Patienten, die bereits gezeigt haben, sind sie stabil mit niedrigen Dosen von Buprenorphin, eine gemeinsame Behandlung von Opioidabhängigkeit, die zuvor nur als lösliche Film- und Tablet war.
Es ist einer der wenigen Medikamente für die Behandlung der opioid Abhängigkeit zugelassen. Die anderen beiden sind Methadon und Naltrexon, letzteres die mit Buprenorphin für einige Opioidabhängigkeit Drogen kombiniert wird.
Ein FDA-Beratungsausschuss gestimmt 12-5 zu Gunsten der Annahme des Implantats im Januar.
Befürworter des Implantats hoffte, dass es die Chancen auf die Droge verringern würde, von Kindern konsumiert oder weiterverkauft und missbraucht.
Diejenigen, die gegen das Medikament die Zulassung gestimmt äußerte Bedenken über die Wissenschaft verwendet, um das Implantat sicher war und die Ausbildung von Ärzten müssten das Medikament Implantat zu beweisen. Einige sagten auch, sie waren besorgt, dass der Ausschuss das Medikament aus der Verzweiflung mehr Behandlungsmöglichkeiten zur Bewältigung der Krise haben genehmigt wurde.
Das Medikament ist von Braeburn Pharmaceuticals hergestellt deren Präsident und CEO von Behshad Sheldon, in einer Erklärung sagte, dass das Unternehmen, dass dies ist das erste was sie hoffen hofft, viele neue Behandlungen zur sucht werden. "Opioidabhängigkeit ist eine chronische Erkrankung und sollte die gleiche Weise behandeln wir andere schwereren, chronischen Krankheiten – mit der Evidenz-basierten Medizin behandelt werden", sagte Sheldon.
Großhandel Probuphine kostet $825 pro Monat, aber es ist noch unklar, wie viel das Implantat kostet, Ärzte und Patienten.
Buprenorphin wurde als Tablette im Jahr 2002 genehmigt. Sucht Spezialisten haben auf besseren Zugang zu der Droge, gefordert, die 100 Patienten nur speziell ausgebildete Ärzte verschreiben können. Sheldon sagte dem Guardian diese Woche, dass Braeburn Gesetzgeber zu Probuphine eine Ausnahme von dieser Mütze machen gekämpft hat.
Ärzte, die das Medikament verschreiben müssen chirurgisch einfügen und entfernen die vier ein-Zoll-lange Stangen ausgebildet sein. Sheldon sagte vorher, ob das Medikament zugelassen wurde, Braeburn 253 Sitzungen, 3.000 Ärzte in den ersten sechs Wochen seine Zustimmung zu trainieren halten würde.