FDA-Sicherheit Warnung: Gefälschte Version von Avastin bei US-Vertrieb
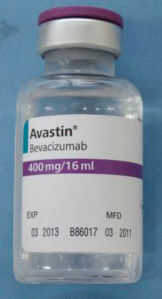
Die US Food and Drug Administration (FDA) warnt, medizinischem Fachpersonal und Patienten über eine gefälschte Version von Avastin 400mg / 16mL, die möglicherweise gekauft und verwendet durch einige Arztpraxen in den Vereinigten Staaten wurden.
Avastin wird ist eine injizierbare Arzneimittel zur Behandlung von Krebs und den Patienten in Kliniken, Krankenhäusern und Arztpraxen. Die gefälschte Version von Avastin enthält keine Wirkstoff des Arzneimittels, Bevacizumab, die bei Patienten, die nicht benötigten Therapie geführt haben kann.
In eine ähnliche Aktion hat FDA Briefe 19 Arztpraxen in den Vereinigten Staaten ausgestellt, die nicht genehmigte Medikamente gekauft, die gefälschte Avastin beinhalten kann. Die gefälschte Version wird als Avastin von Roche hergestellt beschriftet. Roche ist das Unternehmen, Avastin für Marketing außerhalb der Vereinigten Staaten genehmigt.
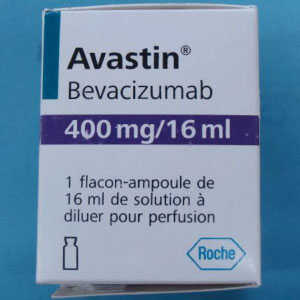
Roche in der Labortests, die die gefälschte Version von Avastin bestätigt. Pakete oder Fläschchen möglicherweise gefälschten wenn sie:
- sind beschriftet mit Roche als Hersteller
- zeigen Sie Batch-Nummern an, die beginnen mit B6010, B6011 oder B86017
Die einzige FDA-zugelassene Version von Avastin für den Einsatz in den Vereinigten Staaten wird von Genentech (ein Unternehmen der Roche) vermarktet. Die FDA-zugelassene Version beinhaltet nicht das Roche-Logo auf der Verpackung oder dem Fläschchen. Genentech FDA-zugelassene Version von Avastin Vials und Verpackung haben darüber hinaus einen 6-stelligen numerischen Batch Nummer und das Ablaufdatum Termine in einem 3-Buchstaben-Monat und 4-stelligen Jahresformat (z. B. JAN 2014). Genentech Avastin-Produkte sind sicher und wirksam für ihre Verwendungszwecke.
19 Arztpraxen in den Vereinigten Staaten gekauft nicht genehmigte Krebsmedikamenten und unter Umständen die gefälschten Avastin aus Qualität Spezial Produkte (QSP), einem ausländischen Anbieter, die auch als Montana Health Care Solutions bezeichnet werden kann. Freiwillige Verteilung in Gainesboro, Tennessee ist ein Distributor von QSP Produkte. FDA hat angefordert, dass die Arztpraxen aufhören verbleibenden Produkte aus diesen Lieferanten. FDA nicht die Sicherheit oder Wirksamkeit des diese nicht genehmigte Produkte gewährleisten.
- Briefe an Ärzte über den Erwerb von nicht genehmigten injizierbaren Krebsmedikamenten

Basierend auf Informationen zu Datum, hat FDA festgestellt, dass keines der nicht genehmigten Krebsmedikamente erhalten durch diese Praxen von Freiwilligen Verteilung in Mangel in den Vereinigten Staaten. FDA-zugelassene Versionen dieser Medikamente gibt es in ausreichende Versorgung, aktuelle Nachfrage zu befriedigen.
Arztpraxen, die nicht genehmigte Produkte aus ausländischen Quellen erhalten haben sollte vor allem aus freiwilligen Verteilung und/oder QSP, nicht mehr verwendet werden und wenden Sie sich an die FDA. Diese Produkte sollten beibehalten und sicher gespeichert.
Melden Sie verdächtige gefälschte Produkte und andere verdächtige nicht genehmigte Produkte freiwillig Verteilung oder QSP/Montana Health Care Solutions oder anderen Quellen entnommen:
- Rufen Sie FDA Büro von strafrechtlichen Ermittlungen (OCI) an 800-551-3989, oder
- Besuchen Sie OCIs-Website (www.accessdata.fda.gov/scripts/email/oc/oci/contact.cfm), oder
- E-Mail: [email protected]
Fachkräfte des Gesundheitswesens und der Verbraucher werden aufgefordert, melden unerwünschte Ereignisse im Zusammenhang mit der Verwendung von verdächtigen injizierbaren Krebsmedikamenten bei der FDA MedWatch Sicherheitshinweise und negative Berichterstattung Veranstaltungsprogramm entweder online, per Post, per Fax oder per Telefon. Health care Profssionals und Verbraucher können entweder:
- Ausfüllen und Absenden der Online-Bericht: www.fda.gov/MedWatch/report.htm, oder
- Download Formular oder rufen Sie 1-800-332-1088 um ein Meldeformular anfordern dann ausfüllen und senden an die Adresse auf dem voradressierte Formular, oder senden Sie per Fax an 1-800-FDA-0178.
FDA weiterhin diese Arzneimittelfälschungen Situation bewerten und Updates informieren.