Flussblindheit Parasit stützt sich auf Bakterien, Host zu täuschen
Auch in der Fremde
Welt der Symbiose, in dem ein paar Organismen auf einander verlassen können
Leben, das hier ist ein Whopper: Bakterien leben in einer parasitären Wurm schaffen
ein Mantel, Abschirmung des Wurms aus dem Immunsystem von seinen Wirten (die, in diesem
Case, erweisen sich als uns).
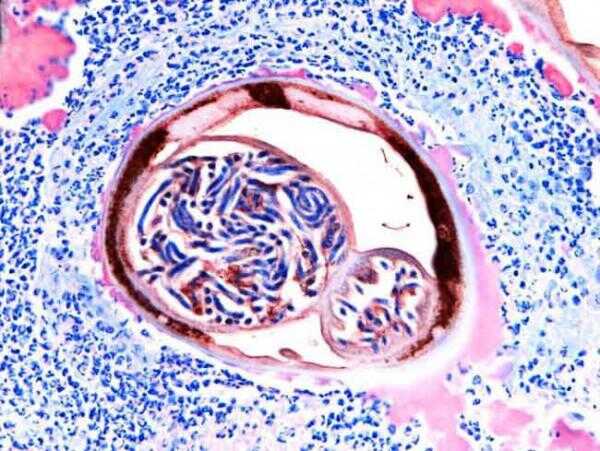
Der Wurm in Frage ist Onchocerca Volvus,
eine parasitäre Nematoden, die Flussblindheit verursacht. Der Wurm wird zu übertragen.
Menschen durch Blackfly beißt, und es hat etwa 18 Millionen Menschen, die meisten infiziert
davon in Afrika. Es verursacht einen juckenden Ausschlag, Knötchen und teilweise 270.000
Blindheit.
"Es ist ein Wurm mit
einem anderen Organismus, so dass der Körper während dieser Infektion irgendwie verwirrt ist
über was zu tun ist es,"Benjamin Makepeace der Universität
Liverpool, der Forschung in die Infektion geführt, sagte LiveScience. "Es hat
sehr ungewöhnlich; die meisten Parasiten, die Menschen infizieren sind ein einziger Organismus."
Sobald dieser ungeraden parasitäre Nematoden jemand infiziert, weißes Blut
Zellen, die sogenannten Neutrophilen, die Bestandteil dieser Person das Immunsystem sind
die Wolbachia-Bakterien zu erkennen und den Wurm-Bakterien-Komplex umgeben. Diese
Neutrophile Angriff der
Bits von Bakterien, die Außenseite zu verweilen, der Wurm, aber sie sind spezialisiert, und
den Wurm selbst angreifen können. Sie sind auch nicht in der Lage, erreichen die
Bakterien auf der Innenseite. Stattdessen sie verweilen und im Wesentlichen bilden einen Mantel um
der Wurm fernzuhalten anderen weißen Blutkörperchen, die es angreifen würde.
"Die körpereigene Immunantwort ist nicht das richtige Ziel sehen. Es wird
auf etwas anderes umgeleitet", sagte Makepeace.
Ein gutes Modell für
Diese Infektion zu studieren kam aus der eng verwandten Onchocerca Ochenai, die Rinder infiziert. Makepeace behandelt
infizierte Kühe mit zwei verschiedene Medikamente. Die Würmer direkt getötet. Die
andererseits ein Antibiotikum tötete die Wolbachia-Bakterien in den Würmern, die wiederum
unter der Leitung
um die Würmer Tod.
Weiße Blutkörperchen genannt Eosinophilen, betrachtet von vielen Wissenschaftlern als nur ein
Aufräum Crew einmal Würmer bereits tot sind, konnte nicht zu handeln, nachdem die Würmer in der
Kuh durch das erste Medikament getötet wurden. Das Vorhandensein der Neutrophilen gestoppt
Sie. Jedoch wenn das Antibiotikum wurde verwendet, um zuerst töten die Bakterien die
Anzahl der Neutrophilen fallen gelassen und die Eosinophilen hereinkam, um das Leben angreifen
Wurm.
"Die Eosinophilen Tötung aktiv beteiligt sind, sondern können nur tun
Wenn die Bakterien Anzahl reduziert worden und die Neutrophilen sind nicht
Da"Makepeace sagte.
Katrin Gentil, ein Onchocerca Forscher an der Universität Bonn in Deutschland,
reagierte auf die Forschung mit den Worten: "The Role of Wolbachia in
immun-Modulation wurde in der Vergangenheit vernachlässigt. Makepeace Gruppe hat gezeigt
die Wolbachia haben eine positive Rolle für den Wurm durch Modulation (in der Hosts
diesem Fall Kuhmilch) Immunantwort. Dies ist ein spannender Roman zu finden. "
Gentil, der ihre Bemerkungen zu LiveScience per E-mail gemacht hat, beteiligte sich nicht an die
Studie.
Frühere Untersuchungen festgestellt, dass der Parasit mit getötet werden können
Antibiotika, aber die Behandlung muss täglich für sechs Wochen verabreicht werden.
Makepeace Team hofft, die antibakterielle Behandlung kürzer, einfacher zu machen
und weniger teuer. Die Forscher arbeiten daran, um ein Wurm-Protein zu entwerfen, die
konnte nach der Infektion des Wirtes "Prime" verabreicht werden
Eosinophile, den Wurm zu töten.
Andere Würmer in der Familie Onchocerca lymphatische Filariose beim Menschen verursachen und
infizieren Sie andere Tiere.
"Das Immunsystem ist wichtig, den Wirkmechanismus von der
Antibiotika,"sagte Makepeace.
- Top 10 geheimnisvolle
Krankheiten - Die
10 die teuflischen und ekelhaft Parasiten - Studie:
Katze Parasiten wirkt sich auf menschliche Kultur
Sie können LiveScience Staff Writer folgen.
Jennifer Welsh auf Twitter @microbelover.