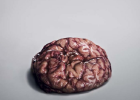
DNA-Reparatur verdient den Nobelpreis in Chemie, und hier ist warum
Gestern der Königlich Schwedischen Akademie der Wissenschaften den Nobelpreis in Chemie, Tomas Lindahl, Aziz Sancar und Paul Modrich für ihre Arbeit bei der Kartierung, wie Zellen zu reparieren beschädigte DNA. Ihre Forschung verbessert unser Verständnis über die Funktionsweise unserer eigenen Zellen und half bei der Entwicklung von Krebs-Behandlungen, aber was bedeutet es wirklich?
Hier ist Ihre Genetik Übersicht

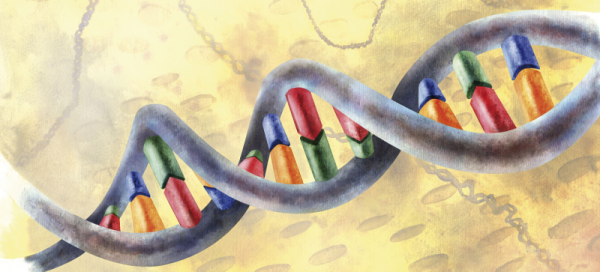
Echte DNA nicht ganz diese ordentlich aussehende. Bild-Gutschrift: gettyimages
Die Anweisungen für den Anbau eines Organismus — Sie, zum Beispiel – befinden sich in ein Molekül namens Desoxyribonukleinsäure, besser bekannt als DNA, die im Zellkern jeder Zelle in Ihrem Körper gespeichert wird. DNA enthält einen genetischen Code, der jede Zelle, welche Art von Zelle sagt zu werden und was Sie mit sich selbst zu tun. Der genetische Code ist nicht in Buchstaben oder Ziffern geschrieben; Es ist in der Chemie geschrieben. Die vier Basen, die Ihr Genom buchstabieren sind Adenin, Cytosin, Guanin und Thymin. Die komplexe Anweisungen für die Entwicklung des Körpers können mit verschiedenen Sequenzen dieser vier Moleküle ausgeschrieben werden.
Sie haben wahrscheinlich bemerkt, dass DNA ein bisschen wie eine kurvenreichen Leiter sieht (Wissenschaftler nennen es eine Doppelhelix, aber "kurvenreichen Leiter" macht mehr Spaß). Die Seiten der Leiter bestehen aus Zuckern und Phosphaten, und die Sprossen bestehen aus Paaren von den vier Basen, die den genetischen Code buchstabieren.
Hier ist, wie alles zusammenpasst. Jede Basis bindet mit einem Zuckermolekül und ein Phosphatmolekül; zusammen bilden sie einen Baustein ein Nukleotids genannt (erinnere mich Nukleotide; wir werden später noch einmal darüber reden). Die Nukleotide Line-up, so dass das Phosphat in ein Nukleotid mit dem Zucker in die nächsten Nukleotids bindet sich an einen langen Strang bilden.
Basen binden mit einander um die Sprossen der Leiter bilden, und die Phosphate und Zucker, die mit ihnen verbunden zu binden, auf die anderen Seite der Leiter bilden. Wenn Ihre Zellen teilen, müssen sie eine Kopie Ihrer DNA für die neuen Zellkern zu machen.
Ein Enzym namens DNA-Helikase wickelt die Doppelhelix und ein anderes Enzym namens DNA-Polymerase (die wir später noch einmal begegnen) bindet neue Nukleotide an die Basen auf jedem Strang. Ein weiteres Enzym DNA-Ligase, dichtet noch oben, drehen Sie die Stränge, und sie zurück in die vertraute Doppel-Helix-Form. Da Adenin immer mit Thymin bindet und Cytosin mit Guanin immer bindet, DNA-Replikation produziert zwei identische DNA-Moleküle — solange nichts schief geht.
Wenn das letzte Teil ein wenig bedrohlich klingt, sorgen Sie nicht allzu viele.
Reparatursysteme in den Zellen
DNA ist Ihr Plan, Firmware und Betriebssystem alle rollte in irgendjemandes, so natürlich ist es sehr wichtig, damit der Code korrekt sein. Aber die Natur der Chemie ist, dass Dinge manchmal schief nach dem Zufallsprinzip gehen. DNA bricht im Laufe der Zeit, manchmal gibt es Fehler bei der Transkription und ultraviolette Strahlung und einige Chemikalien DNA schädigen können. Aber der Körper hat Möglichkeiten, dies zu beheben.
Eiweiß-Molekülen namens Enzyme Act als chemische Reparaturmechanismen für DNA spezialisiert. Wir verstehen, dass einige dieser Mechanismen im Detail auf die chemischen Reaktionen zwischen Molekülen, durch die drei Chemie Nobel-Preisträger, Tomas Lindahl, Aziz Sancar und Paul Modrich. Da Wissenschaftler jetzt verstehen, wie Zellen beschädigte DNA zu reparieren, haben sie auch ein besseres Verständnis der Chemie hinter den Alterungsprozess, einige neurodegenerativen Erkrankungen und verschiedene Arten von Krebs. Das, kann wiederum helfen, effektivere medizinische Behandlungen zu entwickeln.
Das heißt, die Chemie der DNA schädigen und Reparatur ist sehr wichtig und deshalb Lindahl, Sancar und Modrich gewann den diesjährigen Nobelpreis für Chemie. Sie arbeiteten unabhängig voneinander im Laufe der Jahre, anstatt gemeinsam an einem gemeinsamen Projekt, also schauen ihre Nobel-würdige Arbeit individuell.
Tomas Lindahl und DNA-Verfall

Thomas Lindahl. Bild-Gutschrift: gettyimages
Bis Anfang der 1970er Jahre waren Wissenschaftler bequem sicher, dass DNA stabil war. Die Tatsache, dass Leben überhaupt existierte schien gut belegt. Entwicklung hängt gelegentlich Mutationen, weil Mutationen genügend Abwechslung für natürliche Selektion schaffen zu arbeiten, aber Moderation ist der Schlüssel. Wenn genetische Informationen zu viel geändert, allzu oft wäre unmöglich für mehrzellige Lebensformen zu entwickeln in erster Linie es. Stell dir vor, versucht, ein Haus mit einer Blaupause zu bauen, deren Linien halten verschieben oder einer app deren Software-Code ausführen möchten, ändert. Leben würde nie überall bekommen.
Aber in den frühen 1970er Jahren, während Lindahl seine Postdoc an der Princeton University machte er zufällig zu müssen, um eine Probe von RNS, ein Molekül ähnlich der DNA erhitzen die auch genetischen Information trägt. RNA ist nur einem einzigen Strang, keine Doppelhelix wie die DNA, und es nutzt eine Base Uracil statt Thymin genannt. Einige Viren RNA tritt an die Stelle der DNA, und es trägt das Virus genetischen Code. In Ihren Zellen, und die Zellen der meisten anderen Organismen hilft es bei der Replikation der DNA.
Lindahl bemerkt, dass RNA-Moleküle sehr schnell degeneriert, wenn er sie erhitzt. Das machte ihn Wunder wie stabil DNA könnte wirklich sein, wenn die RNA so verletzlich war. Jahre später, konnte während der Arbeit am Karolinska Institutet in Schweden, Lindahl zu beweisen, dass DNA in der Tat im Laufe der Zeit, langsam, aber stetig zerfallen. Diese Entdeckung ist Teil der Grund, warum, den er den diesjährigen Nobelpreis gewonnen.
Das menschliche Genom ist beschädigte Tausende Male jeden Tag. Mit dieser Art von "DNA-Decay", wie Lindahl ausdrückte, den genetischen Code sollte nicht sein stabil genug, um Leben zu entwickeln erlaubt haben — oder beibehalten. Da Leben offensichtlich vorhanden ist, müssen Zellen irgendwie, die ständige Schäden an der DNA zu reparieren.
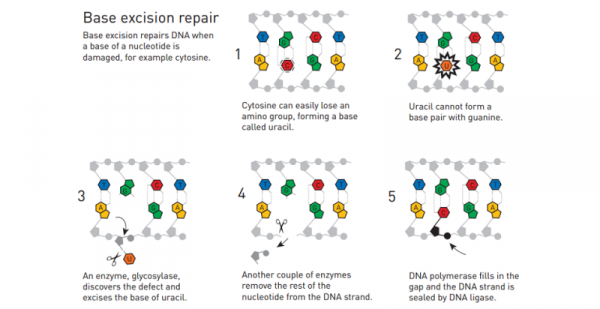
Base Excision Repair. Bild-Gutschrift: Königlich Schwedische Akademie der Wissenschaften
Cytosin, eines der vier Basenpaaren, die hilft, den genetischen Code, buchstabieren verliert oft ein Stück eine Aminogruppe genannt. Ohne dieses Stück Cytosin wird einer anderen Basis: Uracil. Denken Sie daran, dass Cytosin mit Guanin bindet, sondern Uracil (das ist eine der Grundlagen in der RNS) mit Adenin bindet. Und während der DNA-Transkription, bindet Adenin mit Thymin. Das schafft ein DNA-Molekül mit einem anderen Code als das Original: eine Mutation.
Lindahl entdeckt ein Enzym namens Uracil-DNA-Glycosylase (UNG), erkennt die Uracil und schneidet sie aus dem DNA-Strang. Andere Enzyme schneiden Sie den Rest der Uracil Nukleotids, und dann DNA-Polymerase daherkommt und Stecker in eine neue Nukleotid mit einem Cytosin-Basis. DNA-Ligase verschließt sich des Strangs, und es ist so gut wie neu.
Er benannte Prozess base Excision Repair und die Entdeckung in einem 1974 Papier veröffentlicht, und das ist die andere Hälfte des Grundes Lindahl ist jetzt ein Nobelpreisträger. In den nächsten 35 Jahren fand er und viele andere Arten von Glycosylase studierte. Im Jahr 1996 gelang es ihm, den gesamten Prozess in kultivierten Proben menschlicher Zellen neu zu erstellen.
Aziz Sancar und Reparatur von UV-Schäden

Aziz Sancar. Bild-Gutschrift: gettyimages
Als ob es nicht nervenaufreibend genug, die nur DNA-Brüchen nach unten auf seine eigene und muss ein paar tausend Mal am Tag repariert, ist es auch aus externen Quellen, wie ultraviolette Strahlung beschädigt. Hier ist eine Möglichkeit, das funktioniert:
Gibt es zwei Thymin-Basen sitzen nebeneinander in der Reihenfolge, kann UV-Strahlung zu binden mit einander, bilden Paare genannt Dimere, anstatt mit den Basen Adenin gegenüber von ihnen führen. Es ist im Grunde das chemische Äquivalent von einem Doppel-Date schief gegangen, und es setzt einen Anschlag zu DNA-Synthese.
In den 1940er Jahren Wissenschaftler festgestellt, dass Bakterien letalen Dosen von UV-Bestrahlung ausgesetzt unter einfachen alten blauen Licht erholen konnte, aber sie waren nicht sicher, warum. Biologen nannten es Photoreactivation. Fast dreißig Jahre später, erregte dieses Geheimnis die Aufmerksamkeit von jungen Biochemiker namens Aziz Sancar, zusammen mit mehreren anderen Forschern.
Renato Dulbecco vorgeschlagen, dass Photoreactivation stützte sich auf ein Enzym, und Stanley Rupert ihm gab direkt durch die Entdeckung eines Enzyms namens Photolyase und zeigen, dass es funktioniert, um UV-Schäden an der DNA in Bakterien zu reparieren. Aber niemand war noch sicher genau wie Photolyase gearbeitet.
Im Jahr 1978 Sancar gefunden und das Gen, das für Photolyase codiert geklont. Er schaffte es sogar, Bakterien in einer Kultur zu produzieren mehr Photolyase, als sie natürlich würden zu ändern. Dass die Forschung promovierte Sancar, aber er kam nicht mehr zurück zu Photolyase wieder bis 1984, als er an der University of North Carolina in Chapel Hill arbeitete. Dann, in einer Reihe von Papieren in den nächsten Jahren beschrieb er die Chemie, die das Enzym Arbeiten gemacht.
Photylase ist in der Lage, beschädigte DNA zu reparieren, wenn es zu sichtbarem Licht ausgesetzt ist, weil sie können Licht absorbieren und wandeln die Energie in eine chemische Reaktion, die Thymin-Dimere aufteilt. Das ist die Chemie hinter Photoreactivation und entwirren es half Sancar seinen Nobelpreis verdienen.
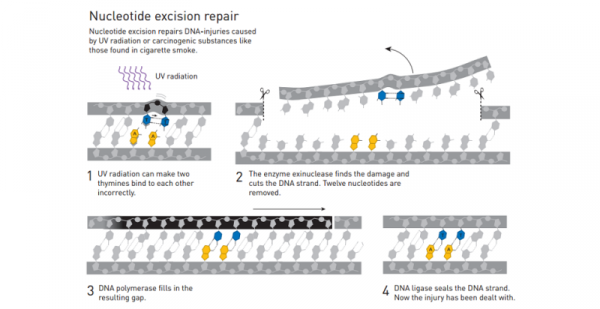
Nucleotide Excision Repair. Image Credit: Königlich Schwedische Akademie der Wissenschaften
Aber es gibt mehr zu der Geschichte. Photoreactivation funktioniert in den meisten Bakterien, aber nicht in Säugetierzellen wie der unsrigen. Unsere Zellen verwenden einen ähnlichen chemischen Prozess, die sogenannten circadiane Uhr eingestellt, aber nicht auf UV-Schäden zu reparieren. Stattdessen verlassen Säugetier-Zellen auf ein Prozess namens Nukleotid Exzision Reparatur, die nicht von Licht arbeiten abhängt. Sancar entdeckt die Enzyme in diesen Prozess eingebunden und im Jahr 1983 veröffentlichte ein Papier beschreibt, wie sie arbeiteten.
Ein Enzym namens Exinuclease bewegt sich entlang der DNA-Strang, bis es eine beschädigte Stück Begegnungen; dann stoppt im Keim erstickt und schneidet den beschädigten Abschnitt aus dem DNA-Strang durch chemische Bindungen zwischen den Nukleotiden zu brechen. DNA-Polymerase füllt die Lücke mit der richtigen Reihenfolge der Nukleotide, und DNA-Ligase Dichtungen bis die reparierte DNA-Strang. Es ist so gut wie neu.
Wir verstehen diesen Prozess dank Sancars Arbeit, und es ist der andere Grund, warum er den Nobelpreis erhielt.
Nucleotide Excision Repair behebt auch andere Arten von Schäden an der DNA, und der Mechanismus ist der gleiche in Organismen von einzelligen Bakterien auf den Menschen; nur die Proteine beteiligt sind unterschiedlich. E. Coli erhält die Arbeit erledigt mit nur drei Proteine, während menschliche Zellen 15 nehmen.
Paul Modrich und Mismatch-Reparatur

Paul Modrich. Bild-Gutschrift: AP Images
Dies kann ein wenig irritierend sein, wenn Sie darüber es zu hart nachdenken, aber die Zellen in Ihrem Körper sind ständig geteilt. Alte Zellen sterben einen programmierten Tod und neue Zellen zu ersetzen. Obwohl es nicht ganz richtig ist, dass Ihre Zellen sich alle 7 Jahre ersetzen, viele der Zellen in Ihrem Körper alle 7 bis 15 Jahre ersetzt zu bekommen.
Bevor eine Zelle sich teilt, es macht zwei Kopien der DNA im Zellkern gespeichert: eine Kopie für jede neue Zelle. Hierzu Moleküle im Zellkern zerreiße die ursprüngliche DNA-Strang und seine zwei Hälften als Vorlagen verwenden, um zwei neue DNA-Stränge zu bauen – einen Prozess namens Transkription. Mit Billionen von Zellen im Körper, jedes geteilt, alle 7 bis 15 Jahre und 3 Milliarden Basenpaare in einem Strang der menschlichen DNA gibt es eine Menge Chancen für eine winzige Abweichung in der Transkription. Und weil wir, Ihren genetischen Code reden, eine kleine Abweichung kann zu großen Problemen führen in Ihrem Körper, wie zum Beispiel Krebs.
Glücklicherweise haben die Zellen eine Möglichkeit der Reparatur der Transkription Fehlanpassungen. Zwei Enzyme, genannt MutS und MutL, bewegen sich entlang der DNA-Strang, Abweichungen zu erkennen. Wenn sie eine Abweichung feststellen, aussortiert ein anderes Enzym namens MutH welche Strang ist das Original und die schlechte Kopie ist. Wie? Der ursprüngliche Strang haben Methyl-Gruppen von Kohlenstoff und Wasserstoff Atome in einer bestimmten Weise angeordnet – befestigt nach außen, während die neueren Strang nicht. Deshalb, weil ein Enzym namens dam Methylase legt Namenscode an der Außenseite des DNA-Stränge, aber es dauert eine Weile, damit auf den ersten, der neuen Strang keine Methyl befestigt. MutH schneidet nicht übereinstimmenden Abschnitt kopieren, und dann die DNA-Polymerase und DNA-Ligase Flicken der Schnitt in der üblichen Weise.
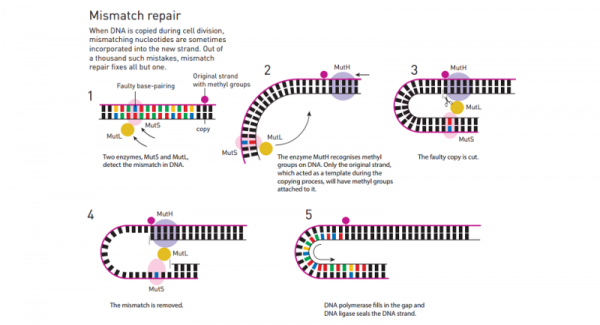
Mismatch-Reparatur. Bild-Gutschrift: Königlich Schwedische Akademie der Wissenschaften
Paul Modrich herausgefunden, dieser Mechanismus und veröffentlichte seine Entdeckung im Jahr 1989, und in diesem Jahr erhielt er den Nobelpreis dafür. Seine Forschungen in den späten 1980er Jahren enthalten Viren mit Fehlanpassungen in ihrer DNA erstellen und dann infizieren Bakterien mit ihnen. Im Inneren der Bakterien, Mismatch-Reparatur die Viren DNA Fehlanpassungen korrigiert, aber nur auf DNA Stränge mit Namenscode befestigt – nicht auf Stränge ohne Methyle.
Einige Fragen über Mismatch-Reparatur sind noch unbeantwortet. Beim Menschen, z. B. Methyl auf der Außenseite der DNA-Stränge hat andere Funktionen, so dass Biologen sind nicht noch sicher wie-Reparatur Mismatch Enzyme erzählen die ursprüngliche DNA-Strang neben der Kopie.
Die Zukunft der Genetik
Wie alle wissenschaftlichen Entdeckungen Lindahl, Sancar und Modrich der Arbeit auf die Arbeit von anderen Wissenschaftlern (viele davon sind auch Nobelpreisträger) gebaut, und wiederum, sie haben ein Fundament an Wissen für zukünftige Wissenschaftler gebaut.
Eine frühere Version dieser Geschichte beschrieben der Basenpaare in der DNA als Aminosäuren. Es wurde korrigiert, zusammen mit der Beschreibung der DNA-Replikation.
Oberes Bild: gettyimages
Kontaktieren Sie den Autor unter [email protected] oder folgen Sie ihr auf Twitter.