Einfache chemische Haltestellen Prion-Krankheit
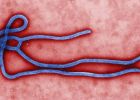
Verrückte Kuh, Scrapie und Creutzfeld-Jakob-Krankheit sind alle Erkrankungen des Gehirns, die Schwächen, bevor sie zu töten, und keine Heilung oder auch viele gute Behandlungsmöglichkeiten über unterstützende Pflege haben. Aber jetzt, sagen Forscher in der Schweiz ist es möglich, blockieren das fehlgefaltete Proteine, sogenannte Prionen, die diese Krankheiten verursachen, mithilfe einer Verbindung, die Biologen verwendet haben, um andere Moleküle zu verfolgen.
Prionen sind eine unterschiedliche Art von Protein – sie können sich selbst replizieren, sagte Adriano Aguzzi, Professor für Neuropathologie an der Universität Zürich, der die Studie leitete. Kommt ein Prion in Kontakt mit ein normales Protein, macht es das normale Protein seine Form zu ändern, und ein Prion, auch. BSE und Scrapie beeinflussen Kühe und Schafe, und Creutzfeld-Jakob-Krankheit (CJK) betrifft Menschen.
In der neuen Studie verwendete Aguzzi Team Chemikalien, so genannte leuchtende konjugierte Polythiophenes, die fluoreszierende Verbindungen, mit denen Forscher oft Gewebeproben, färben sind, damit sie sehen können, was in den Zellen geschieht. Das Team zuerst Mäuse mit einem Prion-Krankheit infiziert, dann mit Polythiophenes injiziert.
Sie fanden heraus, dass einige Polythiophenes verlängert die Mäuse Überleben von mehr als 80 Prozent, im Vergleich zu Kontroll-Mäusen, die nicht mit Polythiophenes injiziert wurden.
Dies bedeutete, dass einige Mäuse überlebt bis zu 140 Tage nach der Infektion, wenn die Polythiophen bekamen vor, mit Prionen infiziert und bis zu 100 Tage wenn sie einmal behandelt wurden infiziert. "Ich war ziemlich überrascht, dass es so gut funktioniert", sagte Aguzzi.
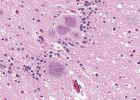
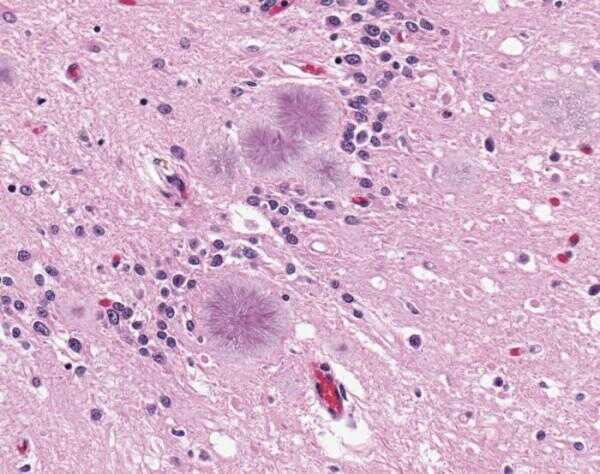
Infektiöse Prionen in das Gehirn nach Menschen oder Tiere essen, die mit ihnen kontaminiert ist. Schließlich, repliziert die Proteine bis zu dem Punkt wo sie Plaques bilden, die Gehirnzellen töten und dem Gehirn das "schwammige" aussehen, die charakteristisch für Prion-Krankheiten (Krankheiten sind formal transmissiblen spongiformen Enzephalopathien genannt) geben kann. [10 Dinge, die Sie nicht über das Gehirn wissen]
Genau wie Prionen die Zellen zu töten ist noch in einige Diskussionen Aguzzi sagte, aber es besteht kein Zweifel, dass Proteine replizieren sie schnell einmal beginnen mit bestimmter Proteine im Gehirnzellen verbinden, und es dauert nur ein paar Prionen um den Vorgang zu starten.
Prionen sind auch wirklich schwer loszuwerden. Die Moleküle sind eng gebunden, sogar kochendes Wasser Temperaturen werden nicht sie aufzubrechen.
In der Studie sagte Aguzzi, das Team hat umfangreiche Computer-Simulationen wie die Moleküle zu interagieren, bevor sie sie in die Tiere, lernen die "Regeln" wie die Chemikalien mit Prionen interagieren gespritzt.
Die Arbeit baut auf Experimente von Beat Meier, ein Forscher an der Schweiz Federal Institute of Technology, sagte Aguzzi. Meier molekulare Bildgebung genutzt, um die Struktur oder infektiöse Prionen im Jahr 2008 zu erfahren. "Niemand sah verbindlich vor, weil niemand wusste, dass die Struktur des Prion vor."
Ein weiterer Schritt war ein Projekt, ein völlig anderes Problem zu studieren. Peter Nilsson, chemischer Biologe an der Universität Linköping in Schweden, experimentierte mit leitfähigen Kunststoffen, aber gefunden, dass eine Chemikalie, die er dachte mit Prionen binden könnte.
Computer-Simulationen zeigten, dass die Polythiophenes tatsächlich in einen Raum passen könnte an einem Ende ein Prion gefunden, und es daran zu hindern, mit normalen Proteinen verbinden.
Es bleibt zu sehen, ob Polythiophenes sicher für Menschen gegeben werden könnte – ihrer Giftigkeit ist noch nicht bekannt, und noch weiter entfernt Tests untersuchen, ob sie in der Hilfe für Menschen mit CJD wirksam sein könnte.
Die Substanzen in neue Studie beschriebenen zeichnen nicht unbedingt diejenigen, die in Menschen treten, "Aguzzi. Die neuen Erkenntnisse zeigen jedoch, dass es gibt einen Pfad zu machen Moleküle, die die Krankheiten Prionen Ursache nicht stoppen konnte.
Die Studie erscheint in der heutigen (5. August) Ausgabe von Science Translational Medicine.
LiveScience auf Twitter folgen @livescience . Wir sind auch auf Facebook & Google +.