Warum "Transgenen Stingray" Schuhe sind wahrscheinlich Fake

Einen anpassbaren Sneaker aus transgenen Stingray Leder gefertigt kaufen wollen? Sie wären besser dran, spart Ihr $1.800 – Wissenschaftler sagen die Ansprüche des Fisches Schuhe das hinausgehen, was mit modernen Gentechnik möglich ist.
Das Thailand-basierten Fisches Schuhwerk sagt, es ist in der Lage, genetisch mix and match Farbmuster von verschiedenen Tieren, transgenen Stachelrochen mit einem Blick auf jeder Schuh Kundenwünsche zugeschnitten zu wachsen. Doch Wissenschaftler sagen, dass die Idee der "Bio-customized" Stingray Leder einen großen Sprung in der Fähigkeit, die viele Gene verantwortlich für Farbmuster manipulieren erfordern würde.
"Zu den besten meines Wissens gibt es keine Möglichkeit zu tun, was sie behaupten beide in Begriffe der Farben, da viele diese Farben auf ihrer Website haben keine Möglichkeit zum Ausdruck gebracht wird, in der Haut und die Fähigkeit, vollständige Kontrolle über das Muster, das sie bedeuten, für alle Tiere, nicht erreicht worden ist", sagte Randy Lewis, Biologe an der Utah State University.
Die transgenen Stingray Anspruch Realitäts-Check aus mindestens zwei Gründen fehlschlägt, sagte Perry Hackett, ein Genetiker an der Universität von Minnesota. Der erste Grund ist, dass Wissenschaftler immer noch Schwierigkeiten einfügen neue genetische Merkmale, die sich viele verschiedene Gene zusammen zu arbeiten, anstatt nur ein einzelnes Gen verlassen haben.
"Der Zustand der transgenen Technologie ist, dass jedes Gen aus einem Organismus in jeder lebende Organismus mit einer hohen Wahrscheinlichkeit verschoben werden kann, dass Sie bekommen, was Sie wollen", sagte Hackett InnovationNewsDaily. "Das Haar in der Suppe hier ist jedoch, dass wenn Sie Dinge wie Muster und dergleichen suchen, das nicht durch ein einzelnes Gen ist. Das ist wahrscheinlich aufgrund vieler Gene, die in gemeinsamer Absprache handelnden."
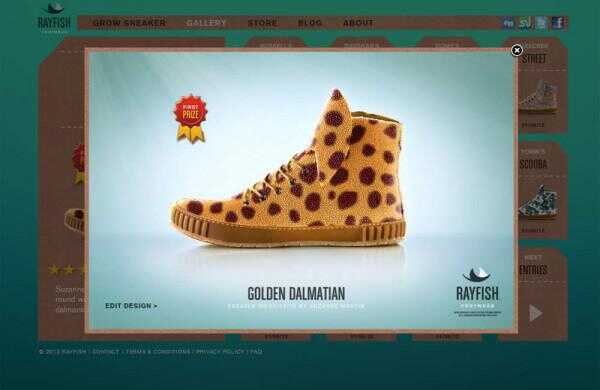
Der zweite Grund für Zweifel Fisches Schuhe Anspruch ist, dass Gene nicht automatisch ihre bestimmten Eigenschaften ausdrücken, wenn in ein völlig anderes Tier gesteckt. Das heißt eine transgene Stingray mit den Genen einen Marienkäfer oder ein Zebra wird nicht automatisch die Haut Muster einen Marienkäfer oder ein Zebra zum Ausdruck bringen.
"Wenn Sie die gleiche Färbung, die ein Schäferhund hat in einem Stachelrochen einführen wollte, es nicht funktionieren würde da das Gewebe eines Hundes, ein Säugetier, aus dem Gewebe von einem Stachelrochen unterscheiden," erklärte Hackett. "So die Regulierung der Gene nicht dasselbe überhaupt sein dürfte, könnte sogar davon aus, dass du etwas zu tun."
Gentechnik hat dennoch einige spektakuläre Ergebnisse erzielt. Wissenschaftler haben einzelne Gene zu Grundfarben bei einigen Tieren zu manipulieren oder zu glühenden Sorten von Hunden und Katzen eingesetzt. Lewis an der Utah State University erstellt transgener Ziegen, Seidenraupen, E.coli-Bakterien und Luzerne in der Lage, Seidenproteine Spinne – Arbeit, die einen holländischen Künstler experimentieren mit "kugelsichere" menschliche Haut inspiriert. ["Kugelsichere Menschenhaut" hergestellt aus Spinnenseide]
Hackett wies darauf hin, dass Menschen in den USA die viel sicherere Investition für den Kauf von transgenen Zebrafisch vermarktet unter dem Namen "Glofish" machen können – aktuelle Sorten sind rot, grün, gelb und lila. Solchen Zebrafisch auch beliebte transgene Tiere in Forschungslabors wie Hacketts darstellen.
Transgenen Technologie in den letzten Jahrzehnten viel besser geworden, sagte Zhanjiang "John" Liu, Molekularbiologe an der Auburn University in Alabama. Aber er wiederholte die Skepsis seiner Kollegen und sagte, dass er die Forschung sichern Fisches Schuhe Anspruch sehen wollen.
"Wenn deine Sachen real ist und deine Sachen den Test der Zeit verträgt, das Zeug da draußen in der Öffentlichkeit und vor [Wissenschaft] Kollegen bekommen", sagte Liu.
Anmerkung des Herausgebers: diese Geschichte wurde bearbeitet, um die zweite Erwähnung von Randy Lewis korrigieren . Er ist Biologe am Utah State University, nicht der University of Utah.
Diese Geschichte wurde von InnovationNewsDaily bereitgestellt , eine Schwester-site zu LiveScience. Folgen Sie InnovationNewsDaily Senior Writer Jeremy Hsu auf Twitter @ScienceHsu. Folgen Sie InnovationNewsDaily auf Twitter @News_Innovation oder auf Facebook.