Was ist der zweite Hauptsatz der Thermodynamik?
Endlose Bewegung zwischen heiß und kalt bedeutet schließlich das Ende des Universums
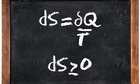
Thermodynamik ist die Studie von Wärme und Energie. Im Zentrum stehen die Gesetze, die beschreiben, wie Energie innerhalb eines Systems, sei es ein Atom, ein Hurrikan oder ein schwarzes Loch bewegt. Das erste Gesetz beschreibt wie Energie nicht erzeugt oder vernichtet, nur aus einer Art in eine andere umgewandelt. Der zweite Hauptsatz ist jedoch wahrscheinlich besser bekannt und noch tiefer, denn er beschreibt die Grenzen dessen, was das Universum tun kann. Dieses Gesetz geht es um Ineffizienz, Degeneration und Verfall. Es sagt uns alles, was wir tun ist von Natur aus verschwenderisch und, dass es irreversible Prozesse im Universum. Es gibt uns einen Pfeil Mal und sagt uns, dass unser Universum ein unentrinnbar düster, trostlose Schicksal hat.
Trotz dieser etwas ernüchternd Ideen wurden die Ideen der Thermodynamik formuliert, in einer Zeit der großen technologischen Optimismus – die industrielle Revolution. In der Mitte des 19. Jahrhunderts, Physiker und Ingenieure bauten Dampfmaschinen zu mechanisieren arbeiten und transportieren und versuchten zu erarbeiten, wie man sie leistungsfähiger und effizienter machen.
Viele Wissenschaftler und Ingenieure, darunter Rudolf Clausius, James Joule und Lord Kelvin, trugen zur Entwicklung der Thermodynamik, aber der Vater der Disziplin war der französische Physiker Sadi Carnot. In 1824 er veröffentlichte Reflexionen über das Motiv Macht des Feuers, die die Grundlagen gelegt, aus Beobachtungen wie Energie rund um Motoren und wie Abwärme bewegt und nützlicher Arbeit bezogen.
Der zweite Hauptsatz kann in mehrfacher Hinsicht, die einfachsten ausgedrückt werden, dass Hitze natürlich aus ein heißer zu einem kälteren Körper fließen wird. Herzstück ist eine Eigenschaft des thermodynamischen Systemen genannt Entropie – in den Gleichungen oben dargestellt wird, durch "S" – locker ausgedrückt, ein Maß für die Unordnung in einem System. Dies in vielerlei Hinsicht, zum Beispiel in der Anordnung der Moleküle – dargestellt werden kann werden Wassermoleküle in einen Eiswürfel mehr als die gleichen Moleküle bestellt, nachdem sie in ein Gas geheizt worden sind. Während die Wassermoleküle in einem genau definierten Gitter im Eisblock waren, schweben sie unvorhersehbar in das Gas. Die Entropie der Eiswürfel ist daher geringer als die des Gases. Ebenso ist die Entropie eines Tellers höher, wenn sie in Stücke auf dem Boden mit verglichen wird, wenn es in einem Stück in der Spüle ist.
Eine formale Definition für Entropie als Wärme bewegt sich um ein System ist in der ersten der Gleichungen gegeben. Die infinitesimale Änderung der Entropie eines Systems (dS) errechnet sich durch Messen, wie viel Wärme ein geschlossenes System (δQ) geteilt durch die allgemeine Temperatur (T) an der Stelle, wo die Wärmeübertragung statt, eingetreten ist.
Die zweite Gleichung ist eine Möglichkeit, den zweiten Hauptsatz der Thermodynamik in Bezug auf die Entropie auszudrücken. Die Formel besagt, dass die Entropie eines isolierten natürlichen Systems immer dazu neigen werden, gleich bleiben oder steigen – das heißt, die Energie im Universum allmählich in Richtung Störung ist. Unsere ursprüngliche Aussage des zweiten Hauptsatzes aus dieser Gleichung ergibt sich: Wärme kann nicht spontan fließen von einem kalten Gegenstand (niedriger Entropie) zu einem heißen Objekt (hoher Entropie) in einem geschlossenen System weil es die Gleichung verletzen würde. (Kühlschränke brechen scheinbar diese Regel, da sie deutlich niedrigeren Temperaturen als die Luft um sie herum, die man einfrieren können. Aber sie nicht das zweite Gesetz verletzen, weil sie nicht isolierte Systeme, erfordern eine ständige Eingabe von elektrischer Energie für Pumpe Wärme aus ihrem Inneren. Der Kühlschrank heizt oben den Raum um ihn herum und, wenn unplugged, würde natürlich wieder thermisches Gleichgewicht mit dem Raum.)
Diese Formel stellt auch eine Richtung auf Zeit; Während jedes physikalische Gesetz die, dem wir kennen, gleich funktionieren würde, ob damals gehen nach vorne oder nach hinten, dies nicht für den zweiten Hauptsatz der Thermodynamik gilt. Egal wie lange Sie es verlassen, dürfte ein kochender Topf mit Wasser immer einen Eisblock geworden. Eine zertrümmerte Platte könnte selbst, nie wieder zusammenbauen, da dies die Entropie des Systems unter Missachtung der zweite Hauptsatz der Thermodynamik verringern würde. Einige Prozesse Carnot beobachtet, sind irreversibel.
Carnot untersuchte Dampfmaschinen, die Arbeiten durch die Verbrennung von Brennstoffen heizt sich auf einen Zylinder mit Dampf, die erweitert und drückt auf einen Kolben dann etwas Sinnvolles zu tun. Der Teil der Kraftstoffenergie, die extrahiert und gemacht, um etwas Sinnvolles zu tun heißt Arbeit, während der Rest der Energie verschwendet (und ungeordneten) ist nennen wir Wärme. Carnot zeigte, dass Sie die theoretische maximale Effizienz einer Dampfmaschine voraussagen könnte, durch die Messung des Unterschied in der Temperatur des Dampfes im Zylinder und die Luft um ihn herum, bzw. im thermodynamischen Bedingungen als die warmen und kalten Reservoir eines Systems bekannt.
Hitze-Motoren arbeiten, weil Hitze natürlich vom heißen zum kalten Orten fliesst. Gäbe es keine kalten Reservoir in die Richtung bewegen könnte gäbe es keine Wärmestrom und der Motor würde nicht funktionieren. Da die Kältespeicher immer über dem absoluten Nullpunkt ist, kann keine Hitze-Motor 100 % effizient.
Die besten Motoren, daher Dampf (oder anderes Gas) auf die höchstmögliche Temperatur erwärmen, dann lassen Sie den Auspuff bei niedrigster Temperatur. Der modernste Dampf, die Motoren zu rund 60 % Effizienz und Diesel-Motoren in Autos bekommen können erreichen rund 50 % effizienter. Benzin-basierte Verbrennungsmotoren sind viel mehr Verschwendung von Energie des Kraftstoffs.
Die Ineffizienzen sind in jedem System mit Energie integriert und thermodynamisch bezeichnet werden können. Diese verschwendete Energie bedeutet, dass die allgemeine Störung des Universums – seine Entropie-Anstieg im Laufe der Zeit aber zu einem bestimmten Zeitpunkt ein Maximum erreichen. In diesem Moment in einigen unvorstellbar fernen Zukunft der Energie im Universum wird gleichmäßig verteilt und so alle makroskopischen Zwecken wird nutzlos sein. Kosmologen nennen dies die "heat-Tod" des Universums, eine unvermeidliche Folge der unaufhaltsamen Marsch der Entropie.













